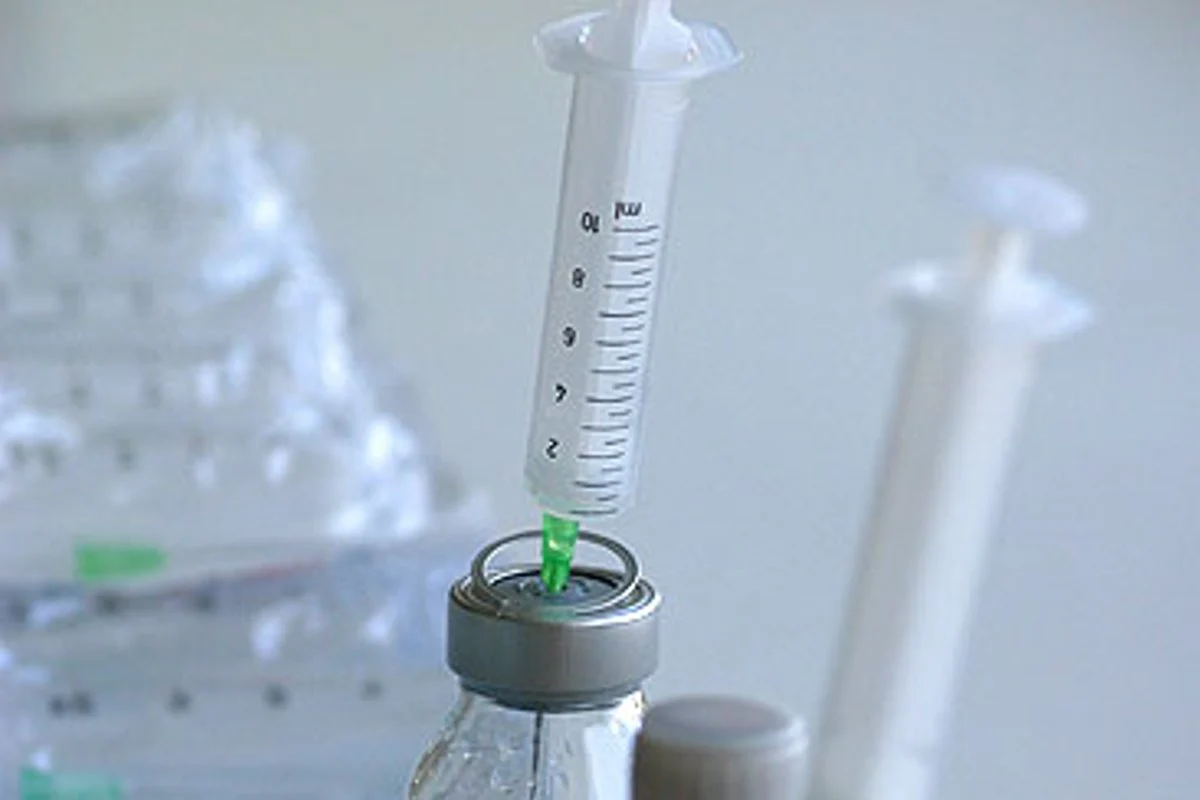
Lietuvos biotechnologijų bendrovė „Sicor Biotech”, gaminanti vaikams skirtą augimo hormoną „Biosoma”, vėl galės juo prekiauti. Tai leido Vilniaus apygardos administracinis teismas, panaikinęs Valstybinės vaistų kontrolės tarnybos sankcijas jo gamintojams.
Saugus ir veiksmingas
Teismas, nagrinėjęs „Sicor Biotech” skųstus Valstybinės vaistų kontrolės tarnybos priimtus įsakymus dėl „Biosomos”, praėjusią savaitę nusprendė, kad jie yra neteisėti.
„Teismas panaikino Vaistų kontrolės tarnybos sprendimą – „Biosomos” pažymėjimas galioja. Vaistas saugus ir efektyvus. Jeigu Vaistų kontrolės tarnyba galvoja kitaip, ji turi viską daryti iš naujo”, – yra sakęs „Sicor Biotech” atstovaujantis advokatas Jaunius Gumbis.
„Sicor Biotech” prekiauti „Biosoma” preparatu buvo uždrausta prieš metus. Valstybinė vaistų kontrolės tarnyba kaltino, kad „Biosomos” veiksmingumas neįrodytas, saugumas neištirtas, o dozavimas nepagrįstas klinikinių tyrimų duomenimis.
Kas penkeri metai
Preparatą „Biosoma”, kuriuo gydomi lėtai augantys vaikai, „Sicor Biotech” gamina nuo 1997 m., kai buvo baigti vaisto klinikiniai tyrimai. Jie buvo atliekami ne tik Lietuvoje, bet ir Latvijoje, Ukrainoje, Baltarusijoje, kitose užsienio šalyse. Tais pačiais metais preparatas buvo įregistruotas Lietuvos vaistinių preparatų registre pagal visus registravimo laikotarpiu galiojusius reikalavimus.
Vaistą „Biosoma” Valstybinė vaistų kontrolės tarnyba perregistravo du kartus – 2002 m. ir 2008 m. Visi Lietuvoje platinami vaistai turi būti perregistruojami kas penkeri metai. Norint pratęsti rinkodaros pažymėjimo galiojimą, Valstybinei vaistų kontrolės tarnybai reikia pateikti atitinkamą dokumentaciją. Tarnyba patikrina vaisto registracijos dokumentaciją, įskaitant ir klinikinių tyrimų kiekį, jų atlikimą ir rezultatus. Tik pripažinusi, kad dokumentacija tinkama ir pagrindžianti palankų vaisto rizikos ir naudos santykį, tarnyba perregistruoja vaistą.
Vertino atgaline data
„Valstybinė vaistų kontrolės tarnyba „Biosomos” klinikinius tyrimus, atliktus 1995–1997 m., vertino pagal reikalavimus, galiojančius dabar, kitaip sakant, pritaikė juos atgaline data, kas nedaroma nė vienoje pasaulio valstybėje”, – taip šį įvykį traktavo „Sicor Biotech” generalinis direktorius profesorius Vladas Algirdas Bumelis.
Tai patvirtina ir Vilniaus apygardos administracinis teismas. Vaisto klinikiniai tyrimai atlikti iki 1998 m. birželio 25 d., kai įsigaliojo Geros klinikinės praktikos taisyklės. Todėl pagal jas „Biosomos” vertinti negalima, nes atliekant tyrimus šios taisyklės negaliojo. Vadinasi, Valstybinė vaistų kontrolės tarnyba neteisėtai išplėtė Geros klinikinės praktikos taisyklių galiojimo ribas laiko požiūriu, ir šias normas taikė procesams, kuriems vykstant jos negaliojo.
Teismas atkreipė dėmesį, kad Valstybinės vaistų kontrolės tarnybos įsakymai buvo nemotyvuotai griežti. Taip pat nurodė, kad vaisto registracija gali būti panaikinta pagal mokslinę išvadą, pagrįstą jo cheminių, farmacinių ir biologinių tyrimų duomenimis, ikiklinikinių ar klinikinių tyrimų rezultatais, bibliografiniais duomenimis ir panašiems dėl šio vaisto neatitikimo nustatytiems reikalavimams.
Neigiamų faktų nebuvo
„Sicor Biotech” generalinis direktorius V.A.Bumelis džiaugiasi teismo sprendimu, nes reabilituotas lietuvių mokslininkų sukurtas vaistas, kuriuo pacientai buvo sėkmingai gydomi ne vienoje pasaulio šalyje daugiau kaip dešimt metų.
V.A.Bumelis primena, kad per visą vaisto platinimo ir vartojimo laikotarpį farmakologinio budrumo sistema neužfiksavo faktų apie neigiamą „Biosomos” naudos ir rizikos santykį.
„Nei mes, vaisto gamintojai, nei kompetentingos Lietuvoje vaistų rinką prižiūrinčios institucijos nėra gavusios nė vieno signalo, kad „Biosoma” neatitinka reikalavimų. Vaisto saugumo faktas patvirtintas stebimais ir fiksuojamais farmakologinio budrumo duomenimis. Periodiškai atnaujinamuose šio preparato saugumo protokoluose nėra užfiksuota nepageidaujamų reakcijų į vaistą „Biosoma” nei Lietuvoje, nei kitose užsienio šalyse, kuriose vaistas registruotas”, – teigia „Sicor Biotech” generalinis direktorius.
Mokslininkai liko įžeisti
Kauno medicinos universiteto Endokrinologijos instituto Bendrosios hormonologijos laboratorijos vadovas profesorius Liudvikas Lašas yra hormoninių preparatų žemaūgiškumui gydyti kūrėjas.
„Šiuos preparatus daug metų kūrėme. Gydėme ir „Biosoma”, ir užsieniniais, gal iš šešių ar septynių pasaulio šalių. Įdomu tai, kad jie niekuo nesiskyrė nuo lietuviškų. Mums tai buvo labai malonu”, – prisimena profesorius L.Lašas.
Jis džiaugiasi, kad lietuviškas vaistas įregistruotas daugelyje šalių ir gautas leidimas juo gydyti. Tačiau, anot profesoriaus, savoje žemėje pranašu nebūsi.
„Galvojome, kad lietuviškas vaistas Lietuvoje yra privalumas, bet, pasirodo, tai yra trūkumas”, – taip profesorius L.Lašas vertina buvusį draudimą pardavinėti „Biosomą”.
Jis stebisi priekabiavimu prie vaisto, nematant esmės, piktinasi metodais, kuriais buvo bandoma sumenkinti ir išstumti vaistą iš rinkos. Natūralu, kad lietuviški vaistai pigesni, bet, anot profesoriaus, prekyba vaistais prilygsta turgaus prekybai.
„Nuleisi kainą – išvarys iš turgaus”, – pelno siekimo ir konkurencijos mechanizmą apibendrina endokrinologijos patriarchas L.Lašas.
Jam apmaudu, kad priekabiaujama prie vaisto, kurį kūrė vien mokslo ir gydymo, o ne komerciniais tikslais.